- 3.1 Efectos de la estructura
electrónica
 Como elementos puros y a temperatura
ambiente, únicamente el hierro, cobalto y níquel
presentan carácter ferromagnético. También
muestran comportamiento ferromagnético algunos elementos
de las tierras raras, pero solo por debajo de la temperatura
ambiente, por lo que tienen escasa aplicación.
Como elementos puros y a temperatura
ambiente, únicamente el hierro, cobalto y níquel
presentan carácter ferromagnético. También
muestran comportamiento ferromagnético algunos elementos
de las tierras raras, pero solo por debajo de la temperatura
ambiente, por lo que tienen escasa aplicación.
 En estos elementos, la fuerte
magnetización se debe a la contribución de los
electrones desapareados de las capas 3d internas, en el caso
de las tierras raras, por los de la capa 4f, cuyos momentos magnéticos
son capaces de alinearse con el campo exterior aplicado, reforzándolo.
En estos elementos, la fuerte
magnetización se debe a la contribución de los
electrones desapareados de las capas 3d internas, en el caso
de las tierras raras, por los de la capa 4f, cuyos momentos magnéticos
son capaces de alinearse con el campo exterior aplicado, reforzándolo.
 El momento magnético que
genera el movimiento de un electrón se conoce con el nombre
de Magnetón de Bhor, de valor:
El momento magnético que
genera el movimiento de un electrón se conoce con el nombre
de Magnetón de Bhor, de valor:
- 1 magnetón-Bhor = qh/4p·me = 9,27·10-24
A·m2
- donde: q es la carga del electrón
 h es la constante de Planck
h es la constante de Planck
 me es la
masa del electrón
me es la
masa del electrón
 En la figura 10.2 se muestra la
estructura electrónica de varios elementos de transición
con orbitales 3d. Recordemos que el criterio de llenado de los
orbitales 3d sigue la regla de Hund, según la cual los
electrones desapareados tienden a presentar sus espines del mismo
valor. De acuerdo con la estructura observada, cada átomo
de hierro puede contribuir a la magnetización con el momento
magnético de cuatro electrones, el níquel con dos
y el cobalto con tres. En cambio, el cobre, al no tener electrones
desapareados, no puede tener carácter ferromagnético.
En la figura 10.2 se muestra la
estructura electrónica de varios elementos de transición
con orbitales 3d. Recordemos que el criterio de llenado de los
orbitales 3d sigue la regla de Hund, según la cual los
electrones desapareados tienden a presentar sus espines del mismo
valor. De acuerdo con la estructura observada, cada átomo
de hierro puede contribuir a la magnetización con el momento
magnético de cuatro electrones, el níquel con dos
y el cobalto con tres. En cambio, el cobre, al no tener electrones
desapareados, no puede tener carácter ferromagnético.
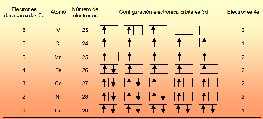
- Figura 10.2 Distribución de espines en las
capas orbitales 3d.
 ¿Que ocurre, sin embargo,
con el manganeso o el cromo? De acuerdo con su estructura, con
cinco electrones desapareados, debería esperarse una magnetización
incluso superior a la mostrada por el Fe. Así ocurre con
un átomo aislado. Sin embargo, en una muestra sólida
de Mn, los átomos se sitúan en la red de tal modo
que los momentos magnéticos de cada átomo se oponen
a los de su vecino, lo que, globalmente, anula la magnetización.
Este fenómeno se denomina antiferromagnetismo.
¿Que ocurre, sin embargo,
con el manganeso o el cromo? De acuerdo con su estructura, con
cinco electrones desapareados, debería esperarse una magnetización
incluso superior a la mostrada por el Fe. Así ocurre con
un átomo aislado. Sin embargo, en una muestra sólida
de Mn, los átomos se sitúan en la red de tal modo
que los momentos magnéticos de cada átomo se oponen
a los de su vecino, lo que, globalmente, anula la magnetización.
Este fenómeno se denomina antiferromagnetismo.
 Aunque su justificación
física cae fuera del objetivo de este curso, podemos señalar
que el fenómeno está asociado con la aparición
de una energía de interacción o de cambio
entre átomos vecinos. Sólo cuando la relación
entre el espaciado atómico en la red cristalina a y el
diámetro del orbital 3d se encuentra entre 1,4 y 2,7 como
muestra la figura 10.3, la energía de cambio es positiva.
Aunque su justificación
física cae fuera del objetivo de este curso, podemos señalar
que el fenómeno está asociado con la aparición
de una energía de interacción o de cambio
entre átomos vecinos. Sólo cuando la relación
entre el espaciado atómico en la red cristalina a y el
diámetro del orbital 3d se encuentra entre 1,4 y 2,7 como
muestra la figura 10.3, la energía de cambio es positiva.

- Figura 10.3. Energía de cambio en función
de la relación entre el espaciado atómico y el
diámetro del orbital 3d.
 Esta distribución espacial
contribuye a disminuir la energía interna y los momentos
de todos los dipolos elementales son capaces de alinearse paralelamente.
Por el contrario, fuera de este rango, la energía de cambio
es negativa y se observa un comportamiento antiferromagnético.
Esta distribución espacial
contribuye a disminuir la energía interna y los momentos
de todos los dipolos elementales son capaces de alinearse paralelamente.
Por el contrario, fuera de este rango, la energía de cambio
es negativa y se observa un comportamiento antiferromagnético.
 Un cambio en la distancia interatómica
puede conseguirse, como sabemos, mediante aleación con
otros elementos o formando parte de estructuras cerámicas,
combinado en forma de óxidos. Estas alternativas permiten
industrialmente aprovechar la respuesta ferromagnética
del manganeso o del cromo, no observable como metales puros.
Un cambio en la distancia interatómica
puede conseguirse, como sabemos, mediante aleación con
otros elementos o formando parte de estructuras cerámicas,
combinado en forma de óxidos. Estas alternativas permiten
industrialmente aprovechar la respuesta ferromagnética
del manganeso o del cromo, no observable como metales puros.



