 Muchos materiales cerámicos
contienen estructuras de silicatos con átomos de silicio
y oxígeno enlazados entre sí en varias distribuciones.
También un gran número de formaciones naturales
de tipo mineral, tales como arcillas, feldespatos y micas son
silicatos. Debemos tener en cuenta que el silicio y el oxígeno
son los dos elementos químicos más abundantes en
la corteza terrestre, de ahí que los silicatos se utilicen
ampliamente en ingeniería oir su bajo precio, disponibilidad,
así como por sus propiedades especiales. Las estructuras
de silicatos son particularmente importantes para materiales
de construcción en ingeniería: vidrios, cemento
portland y refractarios.
Muchos materiales cerámicos
contienen estructuras de silicatos con átomos de silicio
y oxígeno enlazados entre sí en varias distribuciones.
También un gran número de formaciones naturales
de tipo mineral, tales como arcillas, feldespatos y micas son
silicatos. Debemos tener en cuenta que el silicio y el oxígeno
son los dos elementos químicos más abundantes en
la corteza terrestre, de ahí que los silicatos se utilicen
ampliamente en ingeniería oir su bajo precio, disponibilidad,
así como por sus propiedades especiales. Las estructuras
de silicatos son particularmente importantes para materiales
de construcción en ingeniería: vidrios, cemento
portland y refractarios.
 El conjunto básico de
construcción de los silicatos es el tetraedro SiO44-, figura
14.3. El enlace Si-O en la estructura SiO44- es mitad covalente y mitad iónico
y la coordinación tetraédrica del SiO44- satisface los requerimientos
direccionales del enlace covalente y del enlace iónico.
La relación de radios del enlace Si-O es 0.29, que está
en el rango de coordinación tetraédrica para empaquetamientos
compactos de iones estables. A causa del pequeño y muy
cargado ion Si4+, se crean
grandes fuerzas de enlace dentro del tetraedro SiO44-, y como resultado las unidades
de SiO44-
se encuentran normalmente unidas vértice con vértice,
y raramente arista con arista.
El conjunto básico de
construcción de los silicatos es el tetraedro SiO44-, figura
14.3. El enlace Si-O en la estructura SiO44- es mitad covalente y mitad iónico
y la coordinación tetraédrica del SiO44- satisface los requerimientos
direccionales del enlace covalente y del enlace iónico.
La relación de radios del enlace Si-O es 0.29, que está
en el rango de coordinación tetraédrica para empaquetamientos
compactos de iones estables. A causa del pequeño y muy
cargado ion Si4+, se crean
grandes fuerzas de enlace dentro del tetraedro SiO44-, y como resultado las unidades
de SiO44-
se encuentran normalmente unidas vértice con vértice,
y raramente arista con arista.
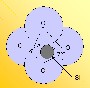
- Figura 14.3. Estructura tetraédrica del SiO44-.
-
 Ya que cada oxígeno del
tetraedro del silicato tiene un electrón disponible para
el enlace, se pueden producir muchas estructuras diferentes de
silicatos. Se producen estructuras de silicatos aislados o
discretos cuando se enlazan iones positivos, por ejemplo
Fe2+, Mg2+
y Ca2+ con los oxígenos
del tetraedro de SiO44-,
para formar unidades de mineral olivino que tiene la composición
química básica (MgFe)2SiO4.
Ya que cada oxígeno del
tetraedro del silicato tiene un electrón disponible para
el enlace, se pueden producir muchas estructuras diferentes de
silicatos. Se producen estructuras de silicatos aislados o
discretos cuando se enlazan iones positivos, por ejemplo
Fe2+, Mg2+
y Ca2+ con los oxígenos
del tetraedro de SiO44-,
para formar unidades de mineral olivino que tiene la composición
química básica (MgFe)2SiO4.
 Si dos vértices de cada
tetraedro de SiO44-
se enlazan con los vértices de otros tetraedros, resulta
una estructura en cadena o en anillo, con la fórmula química
unidad SiO32-,
figura 14.4. El mineral (MgSiO3) tiene
una estructura en forma de cadena y el mineral berilo [Be3Al2(SiO3)6] tiene una estructura de silicato en forma
de anillo.
Si dos vértices de cada
tetraedro de SiO44-
se enlazan con los vértices de otros tetraedros, resulta
una estructura en cadena o en anillo, con la fórmula química
unidad SiO32-,
figura 14.4. El mineral (MgSiO3) tiene
una estructura en forma de cadena y el mineral berilo [Be3Al2(SiO3)6] tiene una estructura de silicato en forma
de anillo.

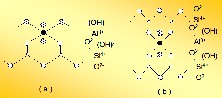
- Figura 14.4. Estructura de silicatos: a) en forma
de cadena, espodumeno, y, b) en anillo, esmeralda.
-
 Las estructuras
laminares de silicato se forman
cuando tres vértices en el mismo plano de un tetraedro
de silicato de enlazan a los vértices de otros tres tetraedros
de silicato. Esta estructura tiene como fórmula unitaria
Si2O52-. Estos silicatos laminares pueden combinarse
con otros tipos de estructuras laminares, al tener todavía
un oxígeno libre. La caolinita, una arcilla común,
figura 14.5a, está compuesta de una lámina de silicato
enlazada iónicamente a una lámina compuesta de
Al2(OH)42+, produciendo delgadas placas de arcilla con
una composición final Al2Si2O5(OH)4. La montmorillonita, o sea Al2(Si2O5)2(OH)2, figura 14.5b, contiene
dos láminas de silicato emparedando a una capa central
de Al2(OH)42+. Estas capas están unidas entre sí
por débiles enlaces de Van der Waals.
Las estructuras
laminares de silicato se forman
cuando tres vértices en el mismo plano de un tetraedro
de silicato de enlazan a los vértices de otros tres tetraedros
de silicato. Esta estructura tiene como fórmula unitaria
Si2O52-. Estos silicatos laminares pueden combinarse
con otros tipos de estructuras laminares, al tener todavía
un oxígeno libre. La caolinita, una arcilla común,
figura 14.5a, está compuesta de una lámina de silicato
enlazada iónicamente a una lámina compuesta de
Al2(OH)42+, produciendo delgadas placas de arcilla con
una composición final Al2Si2O5(OH)4. La montmorillonita, o sea Al2(Si2O5)2(OH)2, figura 14.5b, contiene
dos láminas de silicato emparedando a una capa central
de Al2(OH)42+. Estas capas están unidas entre sí
por débiles enlaces de Van der Waals.
- Figura 14.5. Estructura laminar de los silicatos:
a) caolinita, b) montmorillonita.
-
 Finalmente,
cuando se comparten los cuatro vértices del tetraedro,
se obtiene la sílice, o SiO2. Este material puede
existir en varias formas alotrópicas, ya que al incrementar
la temperatura la sílice, cuarzo a, pasa a cuarzo
b,
y posteriormente se transforma en tridimita b, cristobalita b,
y finalmente a cuarzo líquido. El diagrama de equilibrio
presión-temperatura de la figura 14.6 muestra las formas
estables de la sílice.
Finalmente,
cuando se comparten los cuatro vértices del tetraedro,
se obtiene la sílice, o SiO2. Este material puede
existir en varias formas alotrópicas, ya que al incrementar
la temperatura la sílice, cuarzo a, pasa a cuarzo
b,
y posteriormente se transforma en tridimita b, cristobalita b,
y finalmente a cuarzo líquido. El diagrama de equilibrio
presión-temperatura de la figura 14.6 muestra las formas
estables de la sílice.
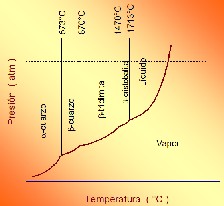
- Figura 14.6. Diagrama de fases presión-temperatura
para el SiO2.
-
 La transformación
de cuarzo a a cuarzo b es una transformación similar a la reacción
martensítica; el cuarzo cambia rápidamente de estructura
cristalina pero genera una ligera distorsión en la red
que implica a los diferentes átomos vecinos, tal como
se indica en la figura 14.7. Transformaciones similares suceden
entre las diferentes formas de tridimita y cristobalita.
La transformación
de cuarzo a a cuarzo b es una transformación similar a la reacción
martensítica; el cuarzo cambia rápidamente de estructura
cristalina pero genera una ligera distorsión en la red
que implica a los diferentes átomos vecinos, tal como
se indica en la figura 14.7. Transformaciones similares suceden
entre las diferentes formas de tridimita y cristobalita.
 Durante
estas transformaciones de fases suceden cambios bruscos en las
dimensiones de los cristales, sobre todo en la transformación
del cuarzo a al b, que producen unas fuertes tensiones internas
que llegan incluso al agrietamiento del material, de ahí
el especial cuidado en la velocidad a la que se producen estos
cambios volumínicos.
Durante
estas transformaciones de fases suceden cambios bruscos en las
dimensiones de los cristales, sobre todo en la transformación
del cuarzo a al b, que producen unas fuertes tensiones internas
que llegan incluso al agrietamiento del material, de ahí
el especial cuidado en la velocidad a la que se producen estos
cambios volumínicos.
 La importancia
que, en la ingeniería y construcción, tienen estos
materiales, hace que estudiemos por separados cada uno de los
grandes grupos en los que se puede clasificar: cemento como constituyente
de los hormigones y morteros, los vidrios tanto de sílice
como modificados, y los materiales silicoaluminosos refractarios
y para construcción.
La importancia
que, en la ingeniería y construcción, tienen estos
materiales, hace que estudiemos por separados cada uno de los
grandes grupos en los que se puede clasificar: cemento como constituyente
de los hormigones y morteros, los vidrios tanto de sílice
como modificados, y los materiales silicoaluminosos refractarios
y para construcción.
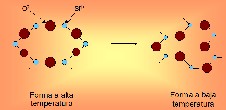
- Figura 14.7. Transformación por desplazamiento
en el cuarzo.









